关于科普下的溶液稀释方法和计算方法,相信很多小伙伴都很有兴趣知道,因为这个话题最近也很火,所以现在大家都想知道科普下的溶液稀释方法。 除了计算,小编还收集了一些科普下溶液稀释的方法和计算的相关资料,分享给大家。
1。 与稀释
相关的概念1.1 稀释
稀释是指在现有溶液中添加更多溶剂以降低其浓度的过程。 稀释后溶液浓度降低,但溶质总量不变。
例如一摩尔(约58.5克)食盐(溶质)溶于一升水(溶剂)中,溶液的体积摩尔浓度为1M,若加入一升水 ,溶液 溶液的体积摩尔浓度变为0.5M,但溶液中盐的总量仍为1摩尔。
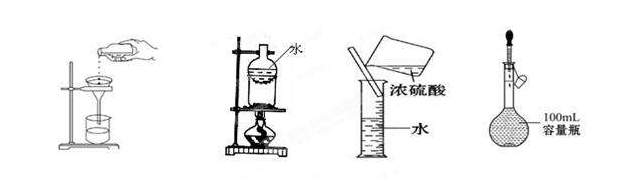
稀释溶液的方法
1.2 溶剂
溶剂是一种能溶解固态、液态或气态溶质,从而变成溶液的液体。 日常生活中最常见的溶剂是水。 所谓有机溶剂,是指含有碳原子的有机化合物溶剂。 溶剂通常具有相对较低的沸点并且容易挥发。 或者它可以通过蒸馏除去,留下可溶物。 因此,溶剂不能与溶质发生化学反应。 它们必须是低活性的。 溶剂可以从混合物中提取可溶性化合物,最常见的例子是冲泡咖啡或茶的热水。 溶剂通常是透明、无色的液体,其中大部分具有独特的气味。
1.3 溶质
溶质,溶液中被溶剂溶解的物质。 溶质可以是固体(例如溶解在水中的糖)、液体(例如溶解在水中的酒精)或气体(例如溶解在碳酸饮料中的二氧化碳)。 事实上,在溶液中,溶质和溶剂只是一组相对概念。 一般而言,量较大的物质称为溶剂,量较小的称为溶质。
1.4 摩尔浓度
摩尔浓度,用 M 表示,是化学中浓度的通用单位。 摩尔浓度定义为构成溶液中某一组分 i 的物质的浓度。 量
除以溶液体积V:
大多数情况下,摩尔浓度是指溶质的摩尔浓度,即溶质物质的量除以溶液的体积 . [小时][小时]2. 溶液稀释方法
溶液稀释方法
2.1 测量:
确定配料罐的容量;
2.2 取液:
]
根据所需配置的浓度要求,设定配料罐浓液液位的设定量;
2.3 移液:
从浓液暂存罐中将浓液泵入配料罐至浓液液位的设定量;
2.4 洗涤:
用蒸馏水洗涤烧杯2-3次,倒入容量瓶中;
2.5 定容:
将水或其他溶剂倒入刻度线1-2cm后,用塑料滴管滴在凹面上笔直;
2.6 充分摇匀:
盖上软木塞,将其倒置,充分摇匀,或用玻璃棒充分搅拌;
2.7 储存:
配料罐中的稀释液可流至储罐储存备用。
